脂肪肝发病年龄日趋年轻化
脂肪肝指由于各种原因引起的肝细胞内脂肪过度堆积。正严重威胁国人的健康,成为仅次于病毒性肝炎的第二大肝病。发病率近年来不断升高,在全球范围内,脂肪肝发病率高达35%。同时,发病年龄也日趋年轻化。
脂肪肝初期症状不明显,大多数患者没有症状,或仅有轻微的疲劳、不适/右上腹部隐痛。但随着疾病的进展,不仅可能导致肝炎、肝硬化损伤肝功能,同时胃肠功能、心血管功能也都会受到影响,最终进展为肝衰竭,威胁生命。
那么,一旦发现脂肪肝,应该如何来干预?如何实现脂肪肝逆转,保护肝功能呢?今天为大家分享一例功能医学成功干预案例。在分享前,我们先一起来简单了解脂肪肝形成的原因。
脂肪肝形成的原因
脂肪肝作为一种复杂的疾病,受到遗传因素和环境因素的共同影响。
遗传因素:双胞胎研究表明,肝脏脂肪含量和肝纤维化具有很强的遗传成分,同时负责肝脏脂质代谢调节蛋白的四种不同基因至少有4种遗传变异和脂肪肝的发生、进展有关。
如果把脂肪肝的遗传因素比作一把上了膛的手枪,那么按下扳机的就是环境因素。脂肪肝受到多种环境因素的影响,如生活方式、肠道菌群、代谢综合征等。根据肝脏中脂肪的代谢路径可以将影响因素分为来源增加、去路受阻两大类。
01
肝脏中脂肪来源增加
肝脏中脂肪常见的来源增加途径主要有3条:
①日常饮食过多摄入。
不合理的饮食结构导致大量外源性脂肪的摄入,超过肝脏的转运能力,导致过多的脂肪在肝细胞沉积,引起脂肪肝。如过度喂养、肠外营养等。
②从头合成途径增加。
体内过多的糖和蛋白质可通过脂肪酸从头合成途径转化为脂肪,导致脂肪过量堆积引起脂肪肝。临床上很多患者反馈日常饮食严格控制脂肪量,依然检查出有脂肪肝,很可能就和过多摄入糖分有关。
③脂肪组织动员。
脂肪组织中储存有大量脂肪,若短时间内动员,排出过多脂肪酸。便可能导致大量脂肪酸沉积在肝脏中。如快速减重导致脂肪动员,短期过多沉积在肝脏中。
02
肝脏中脂肪去路受阻
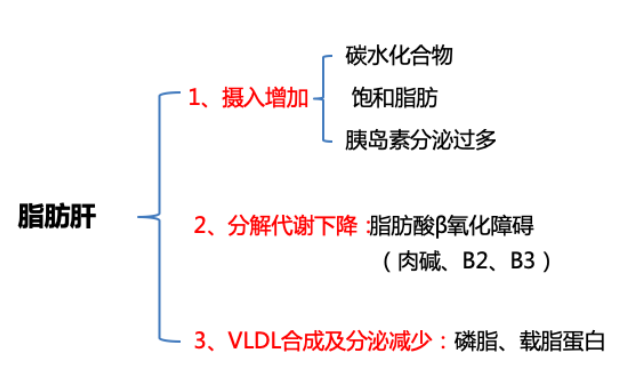
肝脏合成脂肪后,由转运蛋白转移到身体相应部分,发挥功能。肝脏中脂肪主要有2种去路,①经极低密度脂蛋白(VLDL)转运出肝;②经线粒体脂肪酸β氧化供能。两者任一受到影响,均可能导致脂肪不能及时转运,从而引起肝脏中脂肪过多沉积。
①VLDL合成或分泌受损。
肝脏合成的脂肪由VLDL转运出肝脏,如果VLDL(搬运工)合成或分泌受损,导致肝脏中的脂肪不能及时转出,进而引起脂肪肝。载脂蛋白不足、蛋白质营养不良、胆碱缺乏、磷脂不足均可引起VLDL合成或分泌受损。
②脂肪酸β氧化障碍。
脂肪酸β氧化在细胞内线粒体中进行,肉碱不足,导致脂肪酸不能及时被转运至线粒体,会影响β氧化。肠道微生物产生的代谢物NNN-3甲基-5-氨基戊酸会减少肉碱合成,影响脂肪酸氧化,促进肝脏脂肪变性。
维生素B2、B3、B5缺乏、辅酶A缺乏也会引起脂肪酸β氧化受损。同时,脂质过氧化导致线粒体结构异常,影响线粒体功能,也会导致脂肪酸β氧化受损。而在线粒体氧化磷酸化存在缺陷情况下,脂肪酸代谢可能会导致自由基形成增加,肝细胞损伤和纤维化。
脂质过氧化和游离氧自由基会消耗肝细胞内的抗氧化剂,如谷胱甘肽、维生素E、β-胡萝卜素和维生素C,从而使肝脏容易受到氧化损伤。肝脏过多沉积的铁在由Fe3+还原为Fe2+过程中产生自由基,也会消耗抗氧化剂。研究支持抗氧化剂在预防氧化性肝损伤中的作用。
了解原因之后,大致对脂肪肝的干预就有了方向。这样也就能够避免单纯的对症治疗带来的效果不理想。所谓找准病因,药到病除自然也就容易了很多。
功能医学调理案例
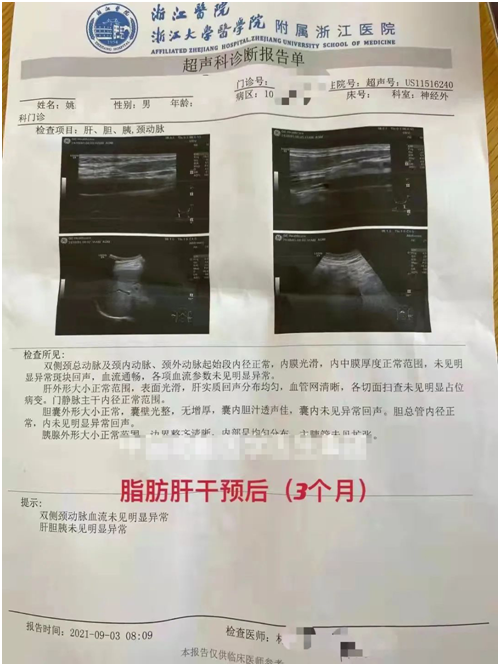
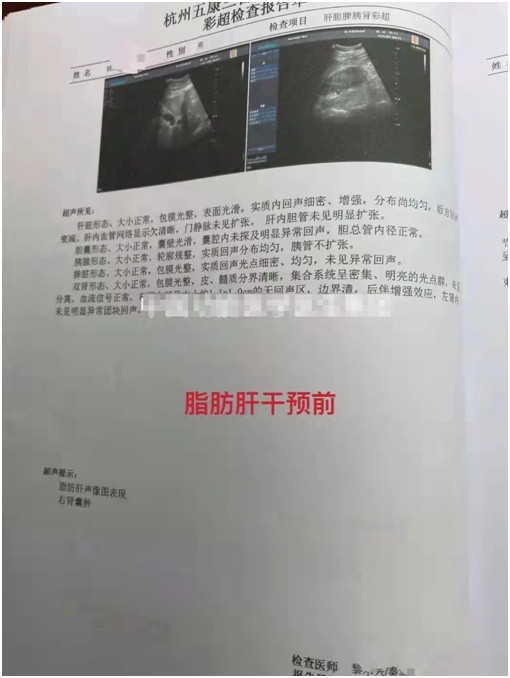
今天的案例的主人公是一名事业有成的男性,57岁,三个月前被诊断脂肪肝。惊喜的是,经过三个月的功能医学方案调理,最近做B超发现脂肪肝已经没有了。
接下来我们一起看看功能医学是如何干预,以达到这样的效果?
第一步
# 收集资料 #
功能医学强调对因治疗,寻找病因的首要任务便是资料收集。所以在患者第一次就诊时,医生采用功能医学矩阵问诊法详细收集患者信息。
第二步
# 综合分析 #
结合矩阵问诊收集信息以及临床检查结果,并完善相应的功能医学检测,综合分析患者脂肪肝出现的原因。发现患者肝脏脂肪代谢的来路和去路都受到了影响。
第三步
# 制定方案 #
根据分析结果制定患者个性化功能医学康复方案。
(1)避免饮食中过多脂肪、能量的摄入
(2)补充脂质代谢需要的营养元素
(3)修复线粒体功能,促进脂肪酸的β氧化
(4)促进VLDL合成;保证足够优质蛋白质摄入;补充VLDL合成过程中需要的营养元素。
(5)补充多种抗氧化剂,清除自由基对肝细胞的损害
第四步
# 效果跟踪 #
方案实施的过程中,根据患者的反应调整康复方案。经过三个月的调理,脂肪肝消失了!